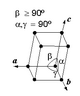
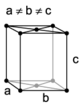
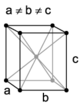
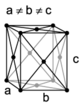
Introducción:
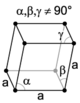
Cada nudo de la red está siendoocupado por un átomo, ión, grupo ionicos o molécula, las cuales se mantiene unidas mediante distintos tipos de enlaces químicos más o menos resistentes.
Además representan la posición de equilibrio que sólo se alcanza totalmente en el cero absoluto de temperatura.También estas partículas las oscilan constantemente de forma que al aumentar la temperatura aumenta la agitación de las partículas, pudiendose producir distosiones de la red o incluso llegar a romperla totalmente.Cuando lo anterior ocurre, se rompen los enlaces químicos que mantenían unido el edificio cristalino y se produce el paso del estado sólido al líquido.
Ejemplo de lo anterior:(manipular el botón)
Hay 5 tipos de edificios , estos son:-
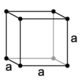
*Edificios Iónicos: Aquí los átomos se mantienen en sus posiciones gracias a la atracción electrostática que se establece entre los iones de carga opuesta, es decir, entre aniones( iones con carga negativa) y cationes( iones con carga positiva ). El enlace iónico se caracteriza principalmente por la transferencia de uno o más electrones de un átomo a otro, que deja carga opuesta en contacto, produciendo un enlace químico muy fuerte. Es posible encontrar estos tipos de enlaces en una gran variedad de minerales, tales como: carbonatos, sulfatos, algunos óxidos, halogenuros , sulfuros, entre otros.Como ejemplo veremos la sal común o halita (NaCl), en donde los iones Cl(-) y Na(+) se destribuyen en posiciones alternantes. Podemos encontrar en la capa externa del anión Cl un electrón en exceso, tomando de la capa más externa de catión Na, que ha quedado con un electrón menos y por lo tanto, con carga positiva.
En estos tipos de edificios, los cationes que ocupan una posición central, donde estan rodeados por un gran número determinado de aiones que define la coordinación o número de coordinación de ese catión.Por lo general se observa un tendencia clara a que los iones se agrupen en estructuras lo más densas posibles, en cualquier caso, el tamaño relativo de los iones influye en la disposición espacial que adopten. Por lo tanto el número de coordinación depende de la relación del radio del catión y los aniones que rodean a este, siendo el radio iónico la distancia desde el centro del núcleo del átomo hasta el orbital más externo. Un catión central grande puede estar rodeado de un mayor número de aniones que un catión de radio pequeño, por ejemplo, si el número de coodinación 4 indica que existen cuatro aniones alrededor de un catión central.
Propiedades de los compuestos con enlaces ionicos:
*El enlace iónico es fuerte, las Uret son muy exotérmicas, lo que implica que cuesta mucha energía romper la estructura cristalina al fundir. Es decir, tendrán puntos de fusión altos.
*Los cristales iónicos son duros, porque el enlace es fuerte y se resisten bastante a ser rayados.
*Sin embargo, son frágiles. Esto es debido a que un golpe puede originar un desplazamiento de los planos de los iones y, al dejar enfrentados iones de igual signo, daría lugar a una fractura en el cristal por fuerzas repulsivas electrostáticas.
*No conducen la corriente eléctrica en estado sólido porque los iones están inmovilizados en la red; pero, al disolverse o fundirse estos iones adquieren movilidad y pueden conducir la corriente eléctrica.
*Se disuelven en disolventes polares, porque los dipolos de estos disolventes rodean a los iones de la red cristalina y los van "arrancando" de la red.

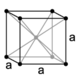
* Edificios Covalentes: Aquí encontramos que los átomos se enlazan compartiendo uno o varios pares de electrones, cuyos orbitales comunes ejercen la acción de enlace.Esto es coún entre los elementos electronegativos, los cuales ceden con dificultad sus electrones, gracias a que los átomos comparten parte de sus envolturas externas de electrones, el enlace covalente es el con mayor fuerza, soliendo así estar dirigido en determinadas direcciones. Un ejemplo de lo anterior es el DIAMANTE,en el cual el átomo central comparte un electrón con cada uno de los átomos que lo rodean y que están localizados en los vértices de un tetraedro como lo es este.
Propiedades de los compuestos con enlace covalente:
Hay que distinguir entre aquellos en los que la formación de enlaces de tipo covalente da lugar a compuestos moleculares y otros en los que se forman redes tridimensionales:
Las redes covalentes se forman por átomos que se unen entre sí por uniones covalentes, por ello la fuerza de unión es fuerte. Las propiedades de este tipo de compuesto vendrán definidas por este hecho:
* Presentan elevados puntos de fusión (generalmente subliman si se sigue calentando)
* Muy poco solubles en cualquier tipo de disolvente.
* Suelen ser duros.
* Suelen ser malos conductores de la electricidad.
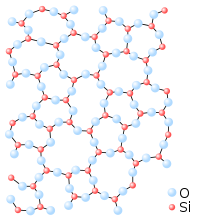
Son sustancias de este tipo el diamante, SiO2 (cuarzo), carburo de silicio (Si2C), nitruro de boro (BN), etc.
Las sustancias covalentes moleculares se caracterizan porque sus átomos se unen mediante enlaces covalentes, pero forman entidades moleculares individuales. Éstas interaccionan entre sí mediante fuerzas intermoleculares, siendo el tipo de fuerza intermolecular presente la responsable de las propiedades que presentan las sustancias:
* Se pueden presentar en estado sólido, líquido o gaseoso a temperatura ambiente. En general, sus puntos de fusión y ebullición no son elevados, aunque serán mayores cuando las fuerza intermolecular que une a las moléculas sea más intensa.
* Suelen ser blandas y elásticas, pues al rayarlas sólo se rompen las fuerzas intermoleculares.
* La solubilidad es variable, siendo solubles en disolventes de polaridad similar. Los compuestos
polares se disuelven en disolventes polares, los apolares en los disolventes apolares.
* En general, son malos conductores de la electricidad. Aunque la conductividad eléctrica se ve
favorecida si aumenta la polaridad de las moléculas.
Son muchas las sustancias de este tipo: H2, Br2, H2O, NH3, compuestos orgánicos, etc.

*Edificios Metálicos: Aquí los nudos de la red cristalina están ocupados por núcleos atómicos rodeados por una nube de electrones, con gran movilidad, que no pertenecen a un átomo concreto, pero que son muy comunes a todos ellos.Estos edificios son propios de elementos poco electronegativos,los cuales liberan con facilidad los electrones de sus orbotales mas externos.Los podemos encontrar en metales, aleaciones naturales y algunos sulfuros y arseniuros.
Poseen gran conductividad eléctrica y térmica, gracias a la gran mivilidad de sus electrones.
Teoría de bandas:
Esta teoría representa un modelo más elaborado para explicar la formación del enlace metálico; se basa en la teoría de los orbitales moleculares. Esta teoría mantiene que cuando dos átomos enlazan, los orbitales de la capa de valencia se combinan para formar dos orbitales nuevos que pertenecen a toda la molécula, uno que se denomina enlazante (de menor energía) y otro antienlazante (de mayor energía). Si se combinasen 3 átomos se formarían 3 orbitales moleculares, con una diferencia de energía entre ellos menor que en el caso anterior. En general, cuando se combinan N orbitales, de otros tantos átomos, se obtienen N orbitales moleculares de energía muy próxima entre sí, constituyendo lo que se llama una "banda"
En los metales existe un número muy grande de orbitales atómicos para formar enlaces deslocalizados que pertenezcan a toda la red metálica (como si fuese una gran molécula). Como el número de orbitales moleculares es muy grande forman una banda en la que los niveles de energía, como se ha dicho anteriormente, están muy próximos.
En los metales se forman dos bandas. Una en la que se encuentran los electrones de la capa de valencia que se denomina "banda de valencia" y otra que se llama "banda de conducción" que es la primera capa vacía.
En los metales, la banda de valencia está llena o parcialmente llena; pero en estas sustancias, la diferencia energética entre la banda de valencia y la de conducción es nula; es decir están solapadas. Por ello, tanto si la banda de valencia está total o parcialmente llena, los electrones pueden moverse a lo largo de los orbitales vacios y conducir la corriente eléctrica al aplicar una diferencia de potencial.
En el caso de los aislantes la banda de valencia está completa y la de conducción vacía; pero a diferencia de los metales, no sólo no solapan sino que además hay una importante diferencia de energía entre una y otra (hay una zona prohibida) por lo que no pueden producirse saltos electrónicos de una a otra. Es decir, los electrones no gozan de la movilidad que tienen en los metales y, por ello, estas sustancias no conducen la corriente eléctrica.
Un caso intermedio lo constituyen los semiconductores, en el caso de las sustancias de este tipo, la banda de valencia también está llena y hay una separación entre las dos bandas, pero la zona prohibida no es tan grande, energéticamente hablando, y algunos electrones pueden saltar a la banda de conducción. Estos electrones y los huecos dejados en la banda de valencia permiten que haya cierta conductividad eléctrica. La conductividad en los semiconductores aumenta con la temperatura, ya que se facilitan los saltos de los electrones a la banda de conducción. Son ejemplos de semiconductores: Ge, Si, GaAs y InSb.
Propiedades de los metales:
*A excepción del mercurio, los metales puros son sólidos a temperatura ambiente. No obstante, sus puntos de fusión son muy variables, aunque generalmente altos.
* Son buenos conductores de la electricidad y del calor.
*Presentan un brillo característico.
* Son dúctiles y maleables. Esto es debido a la no direccionalidad del enlace metálico y a que los "restos positivos" son todos similares, con lo que cualquier tracción no modifica la estructura de la red metálica, no apareciendo repulsiones internas.
*Presentan el llamado "efecto fotoeléctrico"; es decir, cuando son sometidos a una radiación de determinada energía, emiten electrones.
* Se suelen disolver unos en otros formando disoluciones que reciben el nombre de aleaciones.
*Edificios Moleculares: Son propios de las sustancias orgánicas aunque puden darse en algunas ocasines en sustancias inorgánicas como lo es el caso del azufre.Aquí los nudos de la red cristalina están ocupados por moléculas eléctricamente neutras,las cuales se mantienen unidas por cargas eléctricas residuales muy débiles semejantes a las fuerzas de vander waals,propias de los gases.
*Edificios Mixtos: Frecuentemente dentro de un mismo edificio critalino, los átomos, iones o mléculas estén unidos mediante diferentes tipos de enlaces, como por ejemplo el caso del grafito.Dicho mineral contiene únicamente átomos de carbono dispuestos en una estructura laminar y en cada lámina , los átomos de "C" se unen mediante enlaces covalentes, de forma que las láminas son muy fuertes y flexibles, mientras que el enlace que prevalece entre las láminas es un enlace muy débil que facilitando la escamación de dichas láminas, de ahí que la exfoleación sea perfecta a lo largo de estos planos.

El enlace que prevalece en un edificio cristalino determina algunas propiedades de los minerales como por ejemplo: la dureza, conductividad eléctrica, punto de fusión, solubilidad, entre otras.
 Has clic sobre la imagen para verla más grande...
Has clic sobre la imagen para verla más grande...